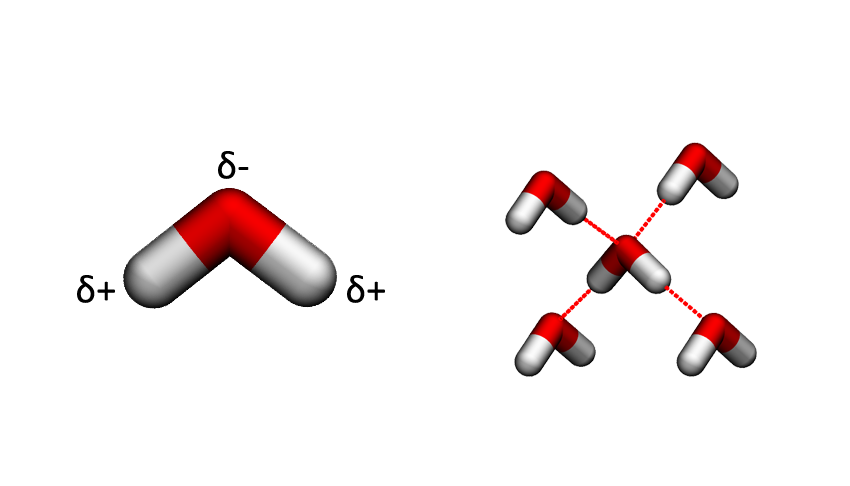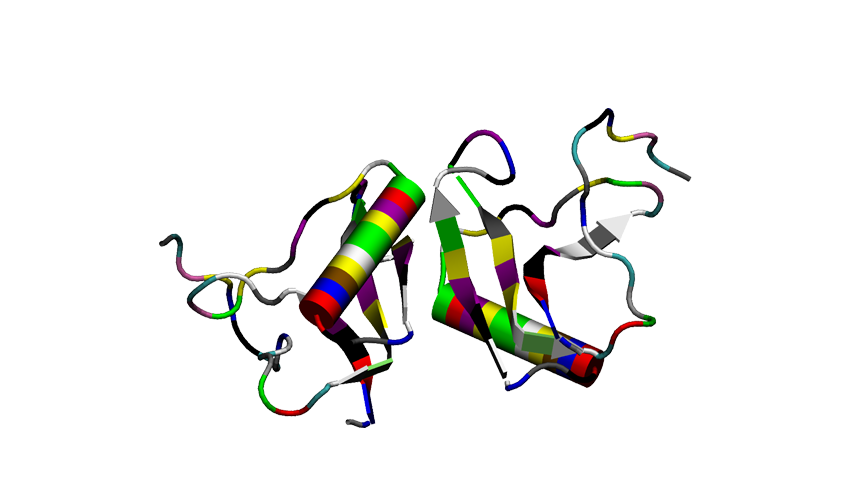
scienceZOOM ©
Už tě někdy napadlo z čeho se vlastně skládá tvoje tělo? Ano, z buněk! Ve svém těle jich v dospělosti máš (velice hrubě odhadnuto) 1‑10.1013, tedy 10 až 100 biliónů! A víš, jak jednotlivé buňky vypadají a z jakých chemických látek jsou složeny? Právě na tuto otázku se ti pokusím dát odpověď.
Díky obrovskému množství chemiků, biochemiků, strukturních biologů a dalších profesí bylo odhaleno mnoho ze struktury a fungování buňky, ovšem ještě více toho stále zůstává nezodpovězeno. Zde ti nabízím malinkou část těchto znalostí, které by tě měly motivovat k hlubšímu studiu.
Každá buňka musí být nějak oddělena od svého okolí. To, že existuje nějaká bariéra, která odděluje "to uvnitř" od "toho venku", je vlastně první předpoklad života. Funkci této bariéry plní buněčná (cytoplazmatická) membrána. Ty nejjednodušší a nejstarší jednobuněčné organismy (složené z jedné buňky) mají pouze tuto membránu a prostor uvnitř není dále rozdělen.
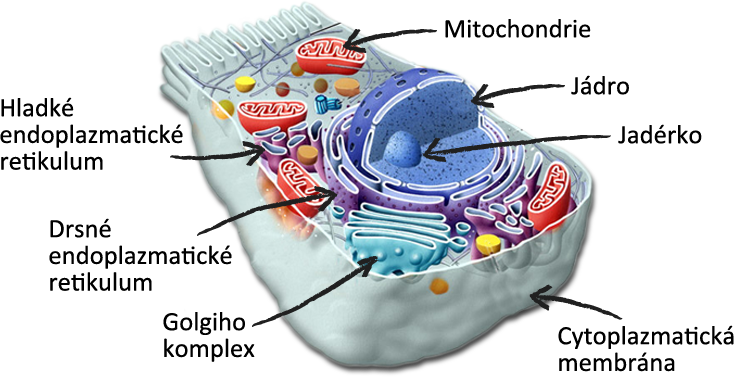
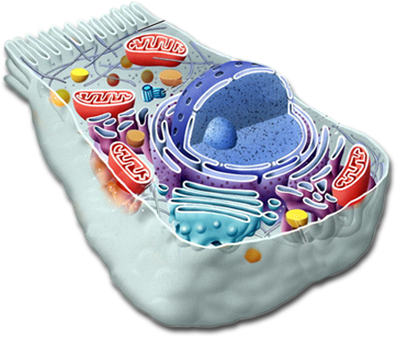
Tyto buňky nazýváme prokariotické. Avšak naprostá většina mnohobuněčných (ale i jednobuněčných) organismů, které vidíš kolem sebe, má vnitřní prostor dále rozdělen na menší části neboli organely. Na některé z těchto organel se podíváme blíže. Řídícím centrem celé buňky je jádro.
V jádře je uložena celá genetická informace v podobě smotané deoxyribonukleové kyseliny, podle níž se řídí výroba mnoha součástek, které jsou k chodu buňky potřeba. Membrána jádra je proděravěná póry, kterými se z něho dostává RNA do buňky. Okolo jádra je poskládáno drsné endoplazmatické retikulum, na které volně navazuje hladké endoplazmatické retikulum.
Slouží jako továrny na výrobu a skladování bílkovin (drsné), a také pro odbourávání toxických látek (hladké). Golgiho komplex je využíván též k úpravě bílkovin, ale také k jejich transportu. Mitochondrie jsou pravými buněčnými elektrárnami. Přijatá potrava se v nich zpracovává na univerzálně použitelný zdroj energie: ATP (adenosintrifosfát).

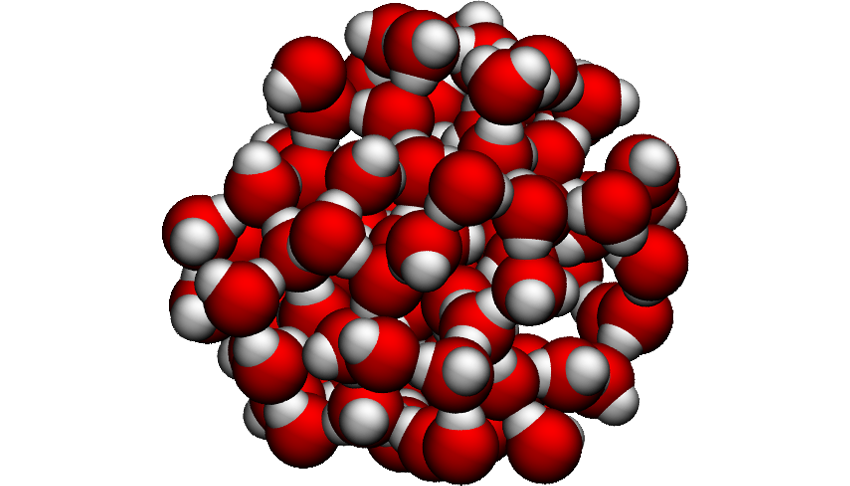
Voda (H2O) je bezesporu nejhojněji se vyskytující molekulou ve tvém těle. U dítěte může tvořit až 75 % jeho hmotnosti, s přibývajícími léty se množství vody v těle ustálí na (průměrně) 60 % hmotnosti těla. Molekula vody je složena z jednoho kyslíku a dvou vodíků.
Vodíky spolu svírají úhel 105° a délka vazby mezi kyslíkem a vodíkem je 0,96 nm (nanometrů, tedy necelá jedna miliardtina metru). Ač je to velmi jednoduchá molekula, její chování je v porovnání s podobnými molekulami (sirovodík - H2S, selan - H2Se, atd.) velmi odlišné. Za to mohou tzv. vodíkové vazby (můstky).
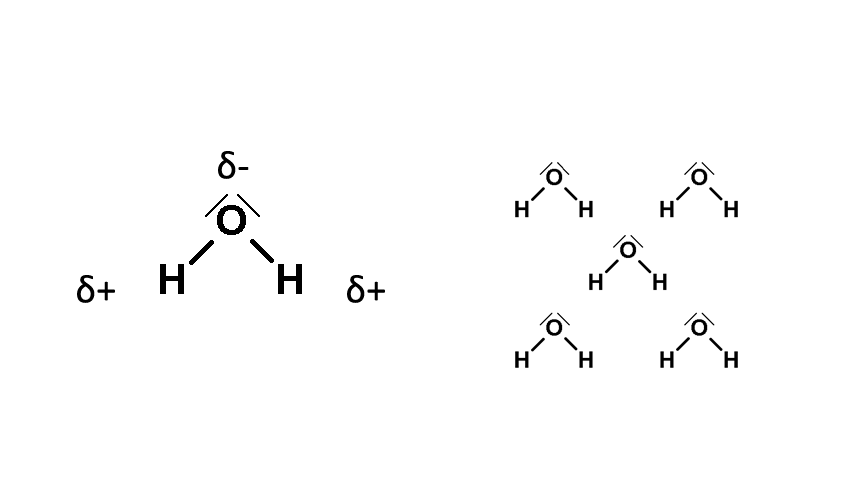
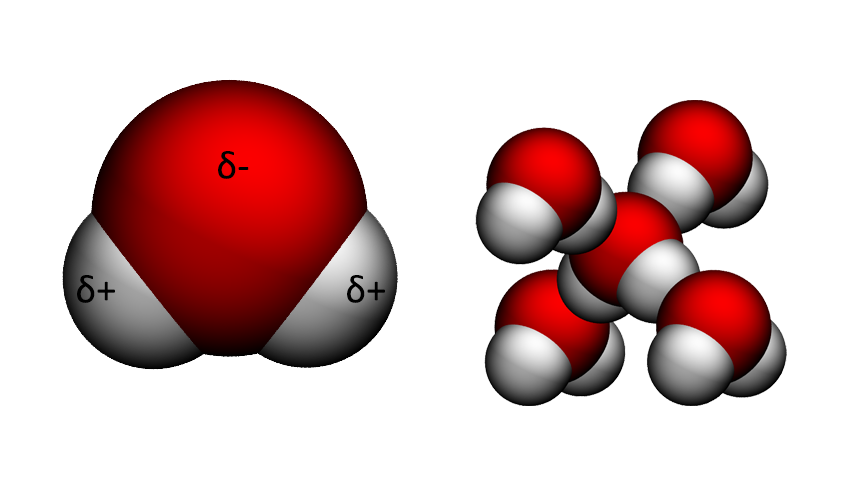
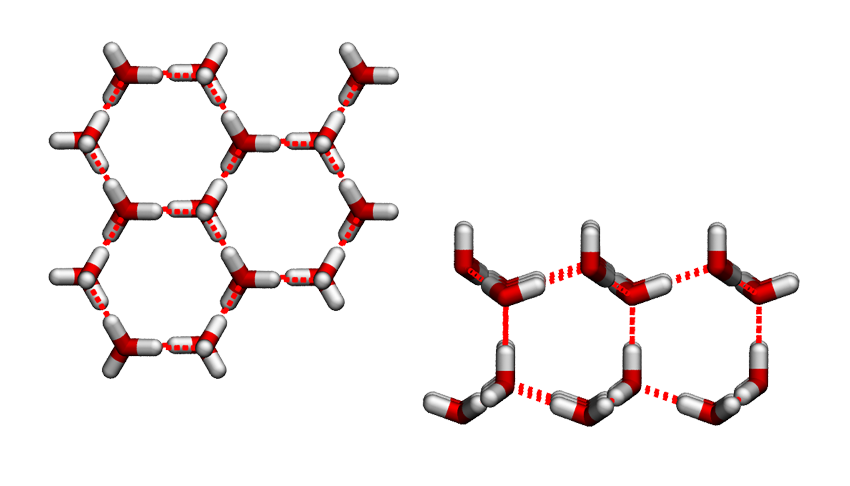
Molekula vody je elektroneutrální, nenese tedy žádný elektrický náboj navíc. Ovšem díky schopnosti kyslíku přitáhnout k sobě část elektronového oblaku z vodíků (říkáme, že kyslík má vysokou elektronegativitu) se na kyslíku vytvoří částečný (parciální) záporný náboj (δ-) a na vodících částečný kladný náboj (δ+). A jak jistě dobře víš, kladný náboj se přitahuje se záporným a naopak.
Proto když se potká jedna molekula vody s druhou, natočí se k sobě tak, jak je to znázorněno na předchozí stránce vpravo - vodík jedné molekuly vytvoří vodíkovou vazbu s kyslíkem druhé molekuly, atd. Pamatuj si tedy, že vodíková vazba se netvoří mezi vodíky, ale mezi vodíkem (navázaným na výrazně elektronegativnější atom) a kyslíkem (nebo dusíkem či fluorem).
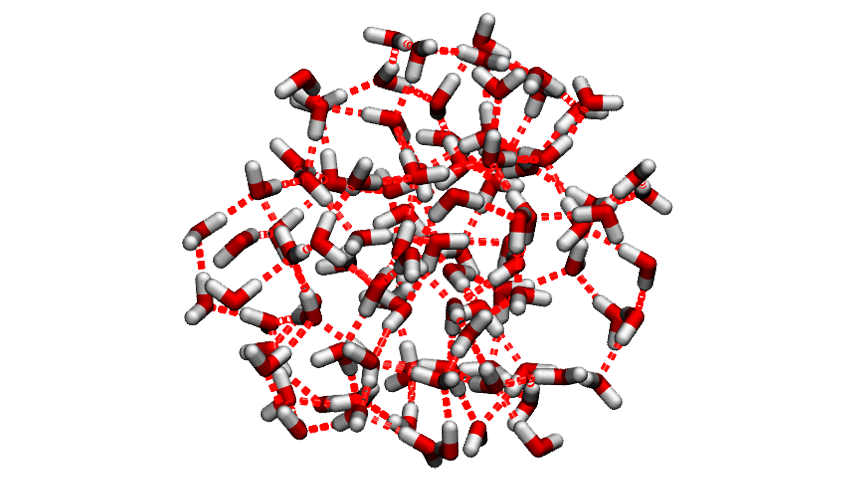
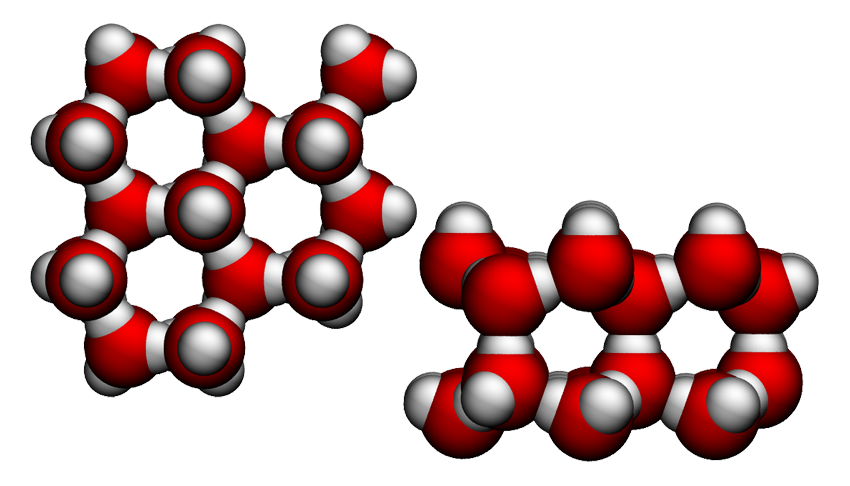
To, že jsou mezi molekulami vody tyto slabé vazby, je příčinou mnoha zajímavých jevů, které u vody pozorujeme. Voda je např. až do teploty 100 °C kapalina, zatímco sirovodík je již od teploty -60,28 °C plyn. Je to tím, že čím více vazeb je mezi molekulami (atomy) a čím jsou pevnější, tím více energie je potřeba dodat, aby se rozbily.
A protože se u sirovodíku vodíkové vazby netvoří, stačí pouze nízká teplota (tedy menší energie) na odpoutání jeho molekul od sebe, což znamená vznik plynu. Díky vodíkovým vazbám a pravidelné struktuře, která se vytvoří při ztuhnutí vody, má pevné skupenství vody - led - menší hustotu, než kapalná fáze (největší hustotu má voda při 3,95 °C). Díky tomu vodní plochy nezamrzají do hloubky a vodní organismy mohou v zimě přežít.
Další důležitou složkou každé buňky jsou ionty. Ionty jsou elektricky nabité částice (atomy i molekuly), které ztratily nebo naopak přijaly jeden čí více elektronů. Ty částice, které ztratily elektron(y) a nesou tedy kladný elektrický náboj, se nazývají kationty, ty, které elektron(y) naopak přijaly a nesou tedy záporný elektrický náboj, se nazývají anionty.
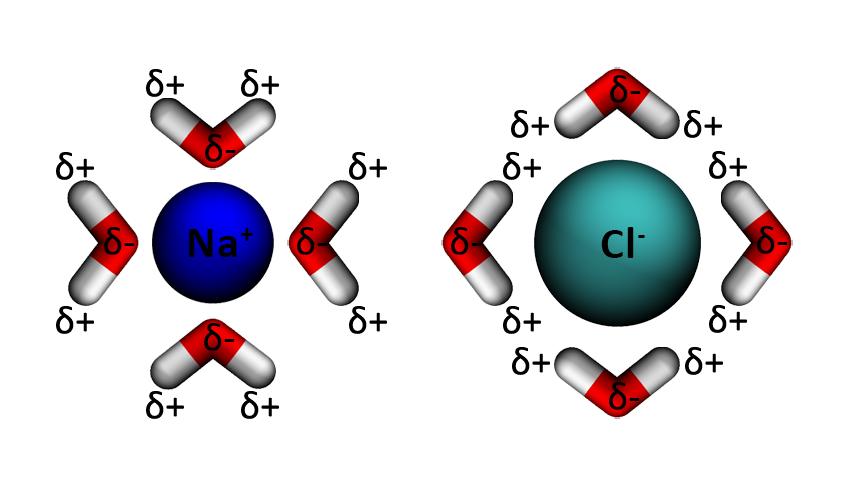
Vzpomínáš si na vodu, která má na kyslíku trochu více záporného náboje a na vodících trochu více kladného náboje? Okolo každého iontu se ve vodě vytváří tzv. solvatační (hydratační) obal, kdy se molekul vody "nalepí" na iont a putují s ním. Orientace molekul vody je znázorněna na obrázku.
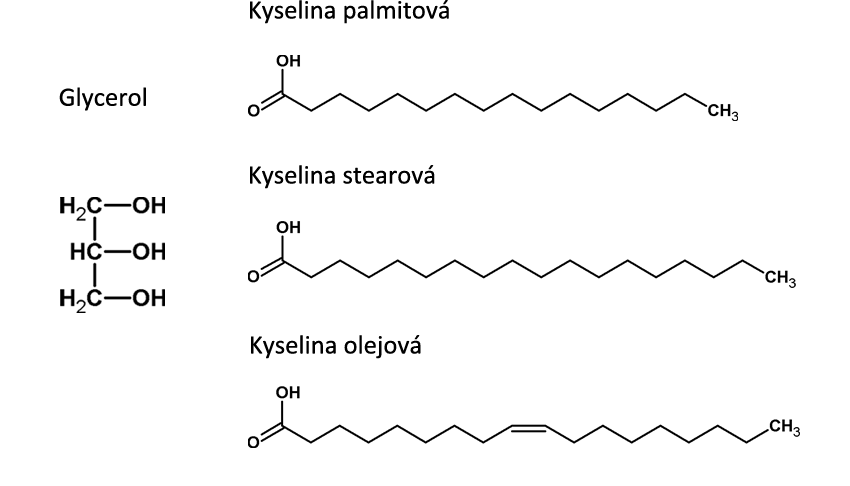
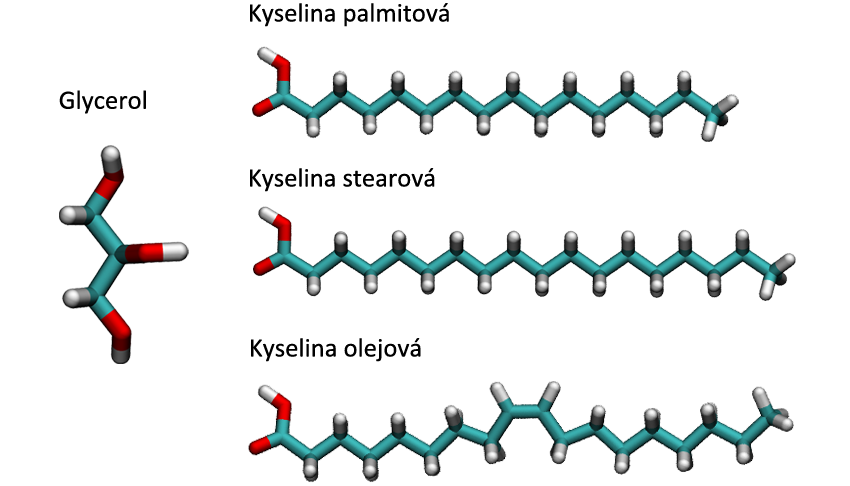
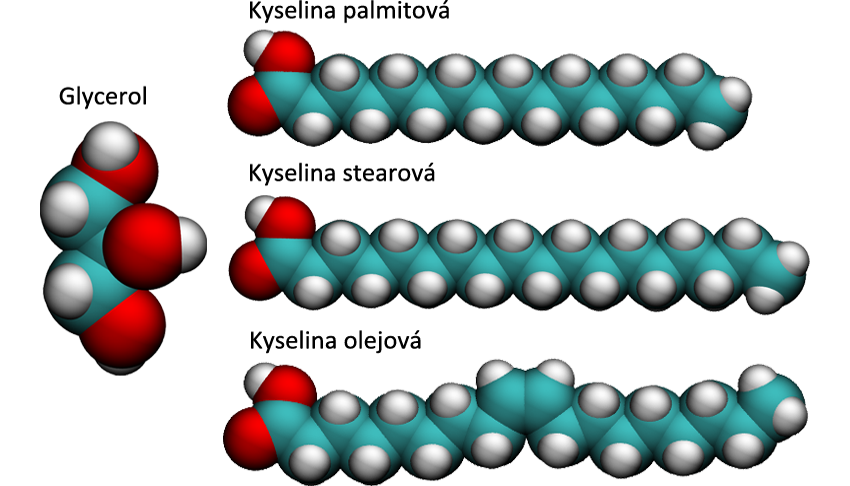
Možná že už i ty jsi se někdy trápil s přebytkem lipidů v oblasti břicha. Ano, lipidy jsou tuky, či přesněji řečeno: tuky jsou podskupinou bohaté skupiny látek, kterou souhrnně nazýváme lipidy. Z chemického hlediska jsou lipidy estery vyšších mastných kyselin s alkoholy. Příklady mastných kyselin vidíš na obrázku vpravo. Jde o dlouhé uhlíkaté řetězce zakončené karboxylovou skupinou -COOH.
Řetězce se mohou lišit počtem uhlíků (kys. palmitová vs. kys. stearová), nebo zastoupením tzv. dvojných vazeb (kys. stearová vs. kys. olejová). Kyseliny, které nemají ve svém řetězci dvojnou vazbu, nazýváme nasycené, a ty, které dvojné vazby obsahují, naopak nenasycené. Příkladem alkoholu, který se v tucích často objevuje, je alkohol glycerol se třemi -OH skupinami.
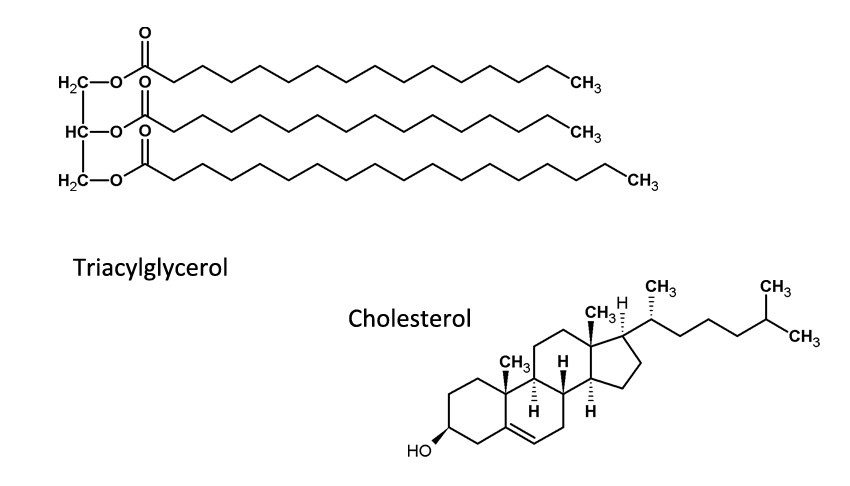
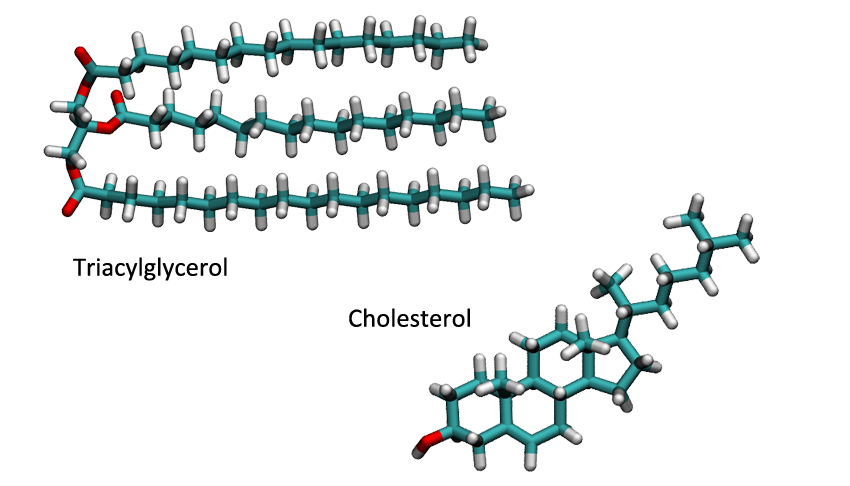
Esterifikací glycerolu s mastnými kyselinami se vytvoří jednoduché lipidy, tzv. acylglyceroly, což jsou právě tuky a oleje. Při procesu esterifikace se spojí alkohol s mastnou kyselinou tak, že se kyslík na alkoholu spojí s uhlíkem karboxylové skupiny za současného odštěpení vody (jeden vodík z -OH skupiny a kyslík s vodíkem z -COOH skupiny).
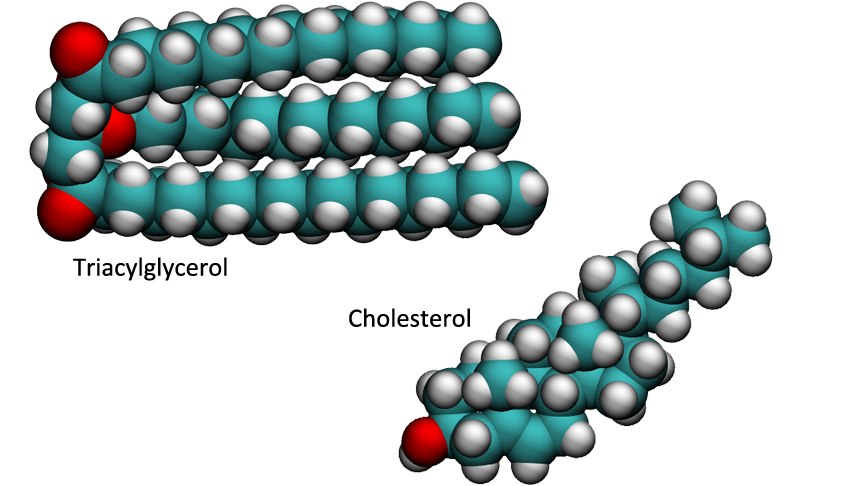
Tyto látky jsou díky vysokému obsahu uhlíku tzv. hydrofobní - nekamarádí se s vodou. Když naliješ olej do polévky, vytvoří se na jejím povrchu mastná oka. A to je právě projevem tohoto nepřátelství, protože molekuly oleje se semknou k sobě, aby měly co nejmenší kontakt s vodou. Další skupinou lipidů jsou isoprenoidní lipidy, mezi něž patří například cholesterol, který je důležitou součástí buněčných membrán.
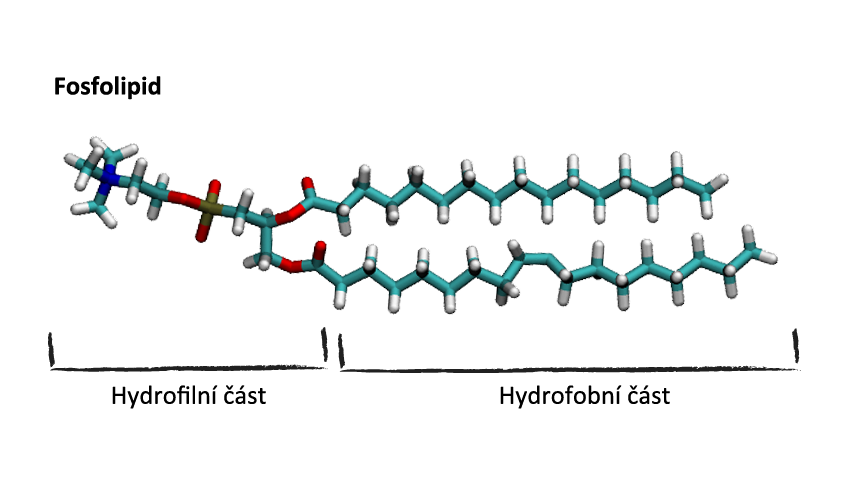
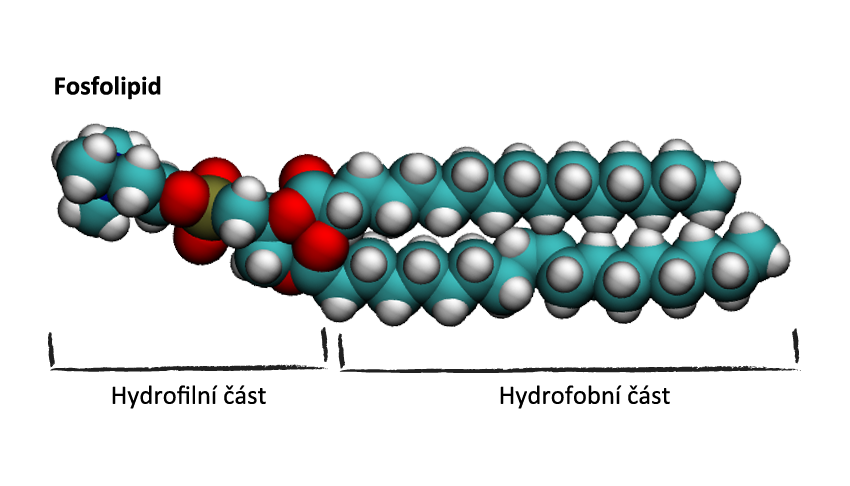
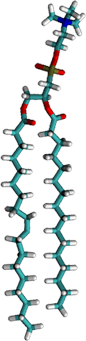
Třetí (z hlediska stavby buňky velice důležitou skupinou) jsou složené lipidy. Když nahradíš jeden uhlíkatý řetězec např. cukrem, vzniknou glykolipidy; když nahradíš řetězec bílkovinou, vzniknou lipoproteiny, a když nahradíš řetězec fosfátem (zbytek kyseliny fosforečné), vzniknou fosfolipidy. A právě fosfolipidy jsou díky své "obojetnosti" velmi zajímavými molekulami.
Nová fosfátová skupina, kterou jsme nahradili původní řetězec, je totiž hydrofilní, tzn. že naopak má vodu velmi ráda. Máme tedy molekulu jak s hydrofobní, tak hydrofilní částí (říkáme, že molekula je amfifilní). A po vložení těchto molekul se začnou dít divy. Začnou se vytvářet různé útvary, kde se dlouhé hydrofobní řetězce shlukují k sobě a naopak hydrofilní hlavičky se snaží dostat co nejblíže k vodě.
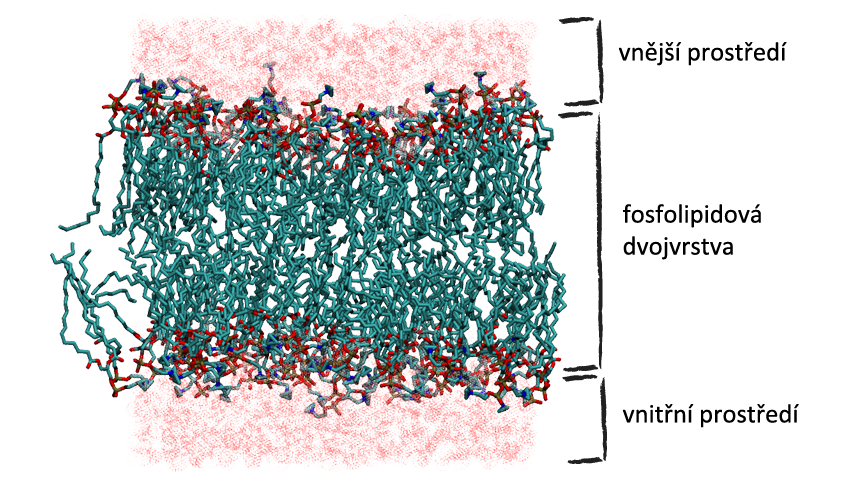
Tyto útvary mohou být buď tzv. fosfolipidové micely nebo tzv. fosfolipidové dvojvrstvy. A právě fosfolipidová dvojvrstva je základem buněčné membrány! Na obrázku vidíš příklad takovéto dvojvrstvy. Z jedné strany je vnitřek buňky, z druhé vnější prostředí. Přes tuto membránu se lehce dostávají plyny a jiné nepolární částice.
Voda už to má o trochu těžší, protože je polární (vzpomínáš si na nerovnoměrné rozložení náboje ve vodě?), a např. ionty, nabité molekuly a velmi velké molekuly se už přes membránu jen tak nedostanou. Např. pro ionty jsou do této dvojvrstvy vloženy speciální kanálky, kterými se mohou přesunout z jedné strany na druhou. Velké molekuly se zase dopravují z vnějšího prostředí do buňky tzv. endocytózou - vchlípením.
Už tě někdy napadlo, proč jsi podobný svým rodičům? Možná, že už ti někdo odpověděl, že za to můžou "gény". Ale kde ty "geny" jsou a jaká je jejich chemická podstata? Každá buňka potřebuje nějakou kuchařku, podle které vyrábí různé molekuly, najde v ní odpovědi na signály, které přijímá ze svého okolí, atd. A právě funkci této kuchařky plní deoxyribonukleová kyselina, neboli DNA.
Tato kuchařka - DNA - je rozdělena do 23 svazků - chromozómů, a každý svazek pak obsahuje několik tisíc receptů, neboli genů. Těchto receptů máš celkem asi 25000 a navíc jich máš naprostou většinu dvakrát - jeden recept od otce a druhý od matky. To proto případ, kdyby byl jeden recept nefunkční.
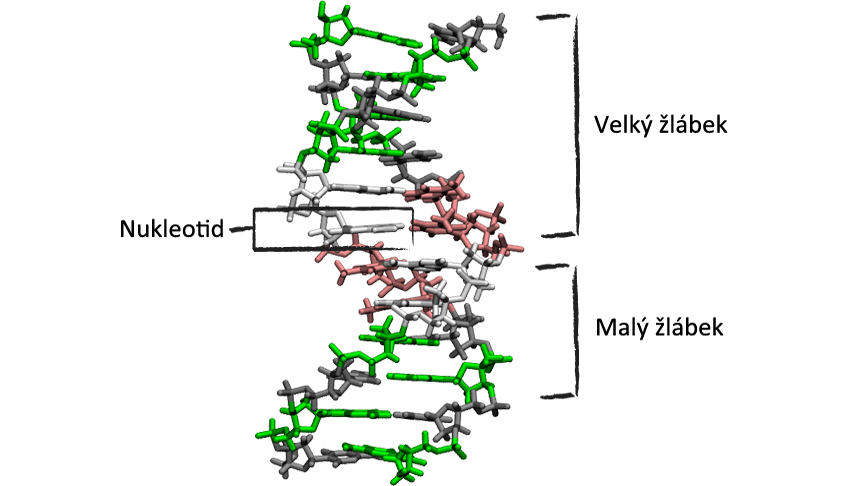
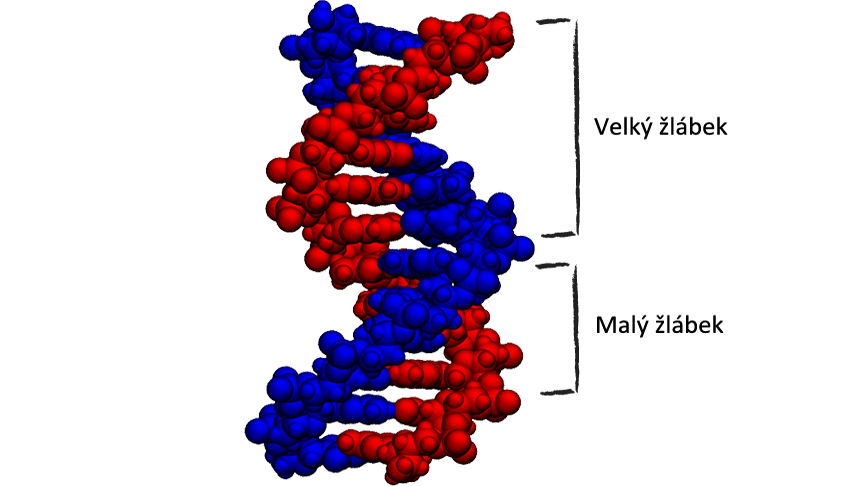
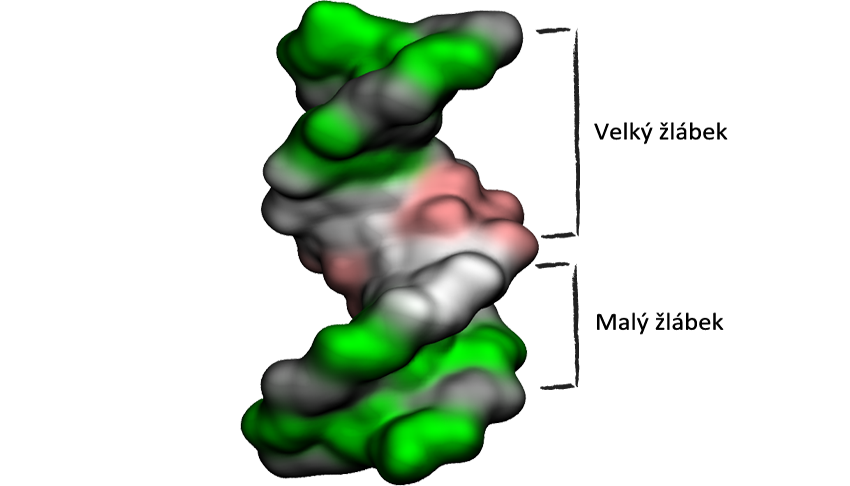
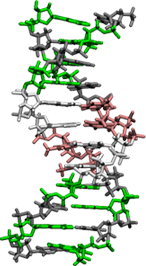
DNA je složena ze dvou vláken, která se navzájem obtáčejí. Vlákna jsou tzv. komplementární, tedy jedno vlákno je doplňkem k tomu druhému. Každé vlákno je jako náhrdelník, na kterém jsou navlečeny korálky čtyř barev v určitém pořadí. Tyto korálky nazýváme nukleotidy a na všech 46 vláknech jsou těchto korálků asi 3 miliardy! Kdybys dal tato jednotlivá vlákna za sebe, pak by měřila asi 1 m!
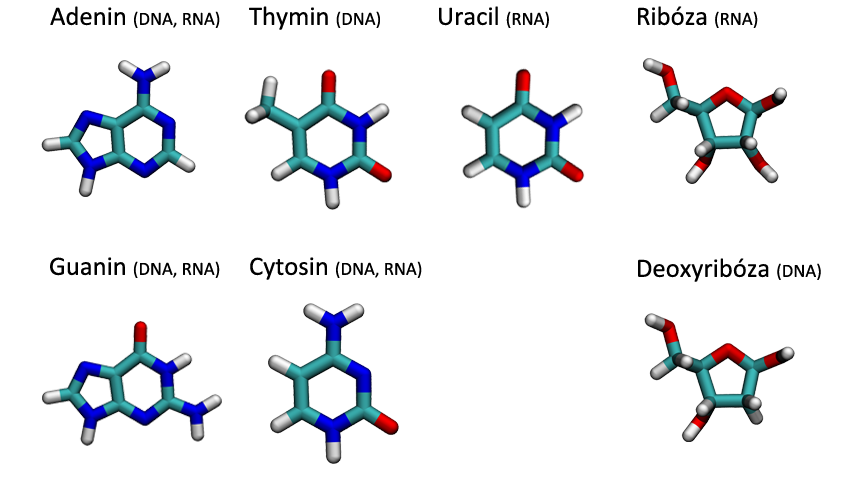
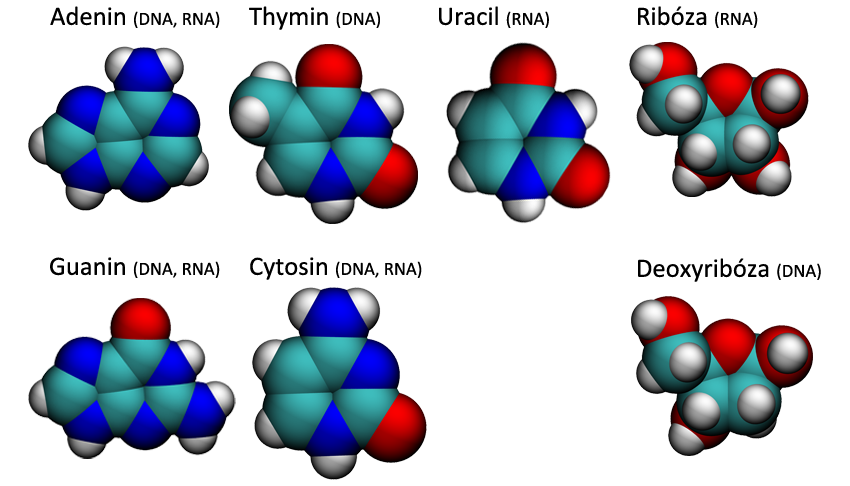
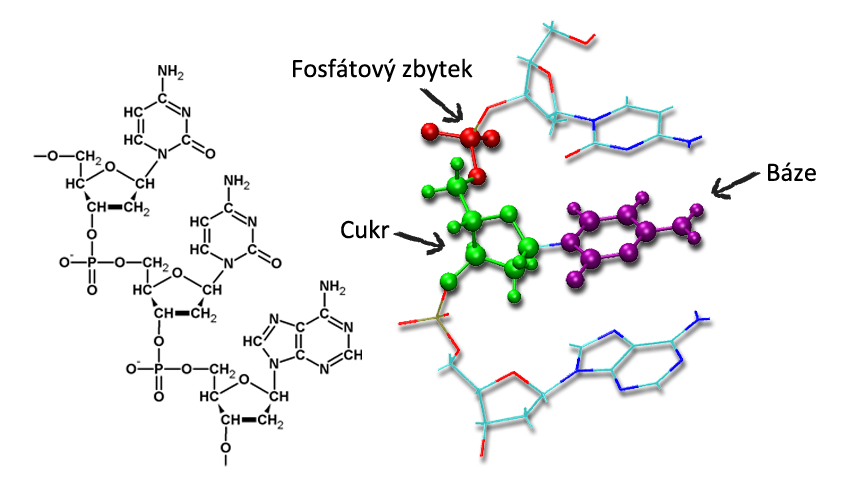
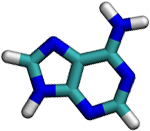
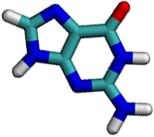
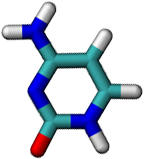
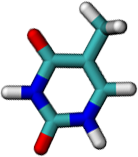
Každý nukleotid je tvořen ze 3 částí. První je tzv. báze, což je (chemicky vyjádřeno) heterocyklická sloučenina na bázi pyrimidinu či purinu. Tyto báze jsou u každého typu nukleové kyseliny čtyři (počkej si na další stránku). Druhou důležitou částí je cukr, buď ribóza nebo deoxyribóza. A třetí je zbytek kyseliny fosforečné H3PO4.
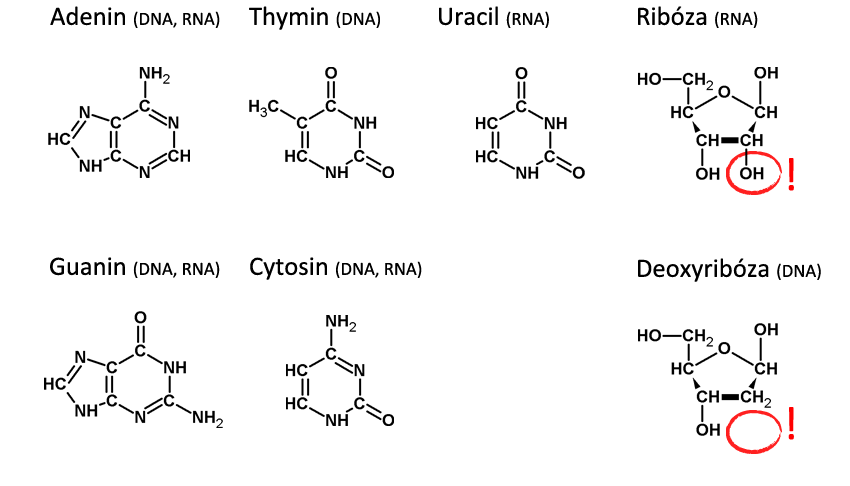
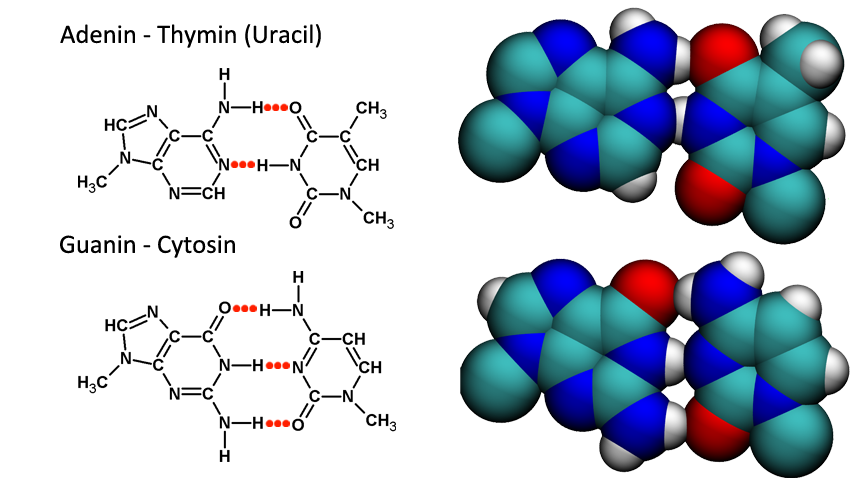
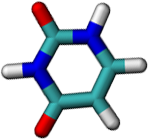
Všimni si, že thymin spolu s uracilem a cytosinem mají podobnou strukturu a adenin je podobný zase guaninu. První tři patří mezi tzv. pyrimidinové báze, které jsou tvořeny jedním šestičlenným kruhem, a další dva patří mezi tzv. purinové báze, u kterých je k jednomu šestičlennému kruhu přilepen menší pětičlenný.
Kostru mají tedy vždy tyto tři a dvě báze podobnou, liší se však bočními skupinami. Je to buď aminová skupina -NH2, nebo kyslík =O, nebo methyl -CH3, a nebo jenom vodík -H. Podle typu cukru rozlišujeme dva typy nukleových kyselin: kyselinu ribonukleovou (RNA), kde se využívá cukr ribóza, a kyselinu deoxyribonukleovou (DNA), kde použitým cukrem je deoxyribóza.
U cukrů jde na první pohled o malou změnu - deoxyribóze chybí jedna -OH skupina, ovšem po chemické stránce se tím velmi změní vlastnosti celé kostry. Kostra DNA je pevnější a chemicky stabilnější než u RNA, proto je právě DNA hlavním "mozkem" buňky a RNA slouží jako její posel, který doručuje informaci do různých koutů buňky. Navíc u RNA se místo báze thyminu vyskytuje spíše báze uracil.
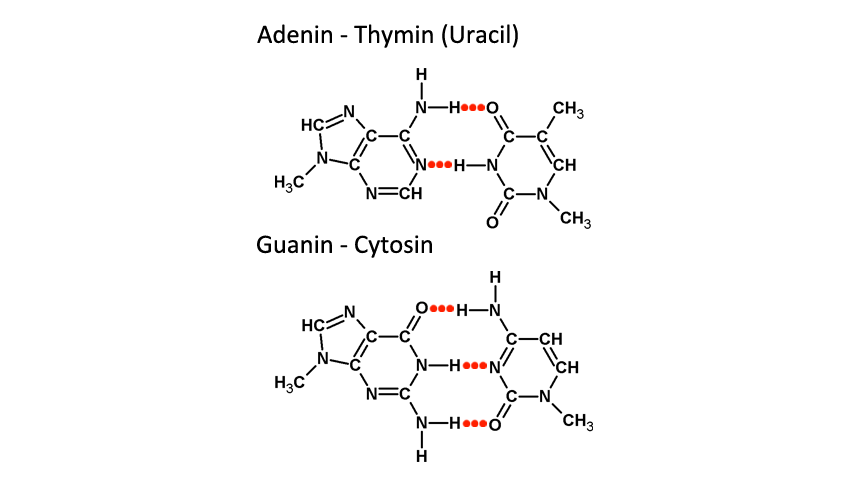
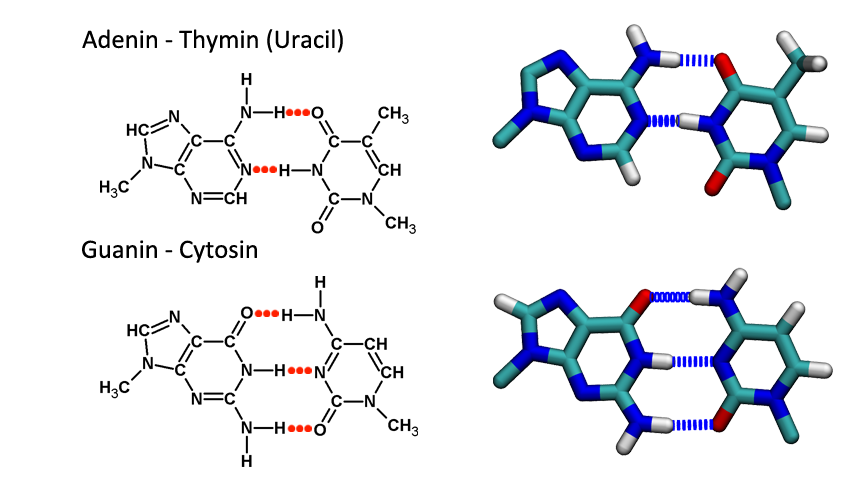
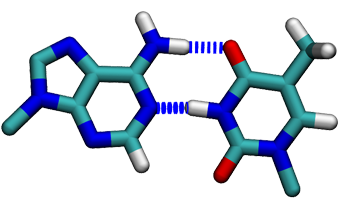
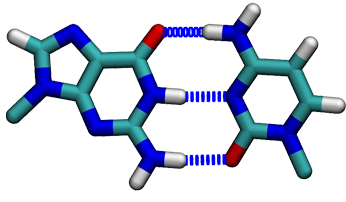
Dříve zmíněné báze spolu vytváří tzv. komplementární páry. Vždy jedna pyrimidinová se páruje s purinovou a naopak. Adenin se páruje s thyminem (nebo uracilem u RNA) a guanin s cytosinem. Mezi oběma bázemi se vytváří dvě nebo tři vodíkové vazby a ty zaručují, že dvojšroubovice DNA drží u sebe.
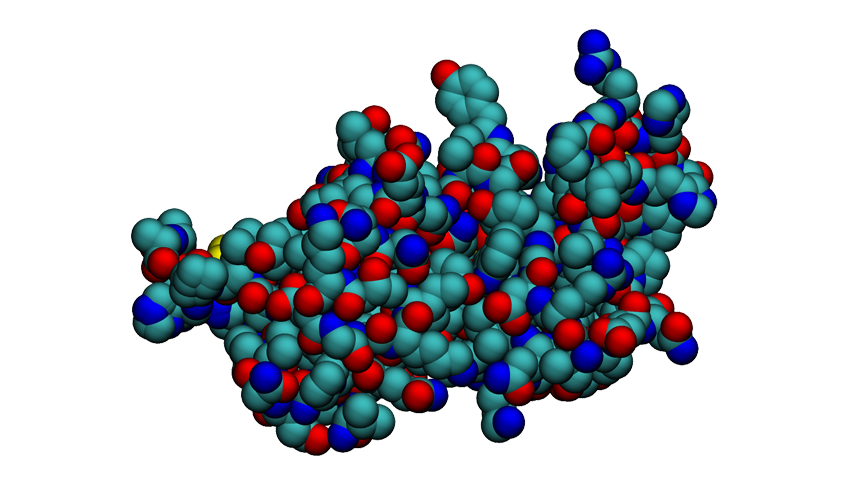
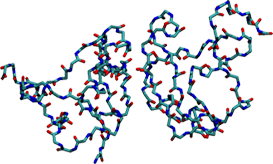
Jestliže lipidy jsou stavebními kameny buněčných membrán (a vydatným zdrojem energie) a nukleové kyseliny mozkem buňky, pak bílkoviny (nebo také proteiny) jsou hlavní pracovní silou buňky. Podílejí se na transportu látek přes membrány i v rámci buňky, zajišťují pohyb buňky, slouží jako katalyzátory reakcí, podílejí se na obraně buňky, řídí a regulují mnohé procesy v buňce atd.
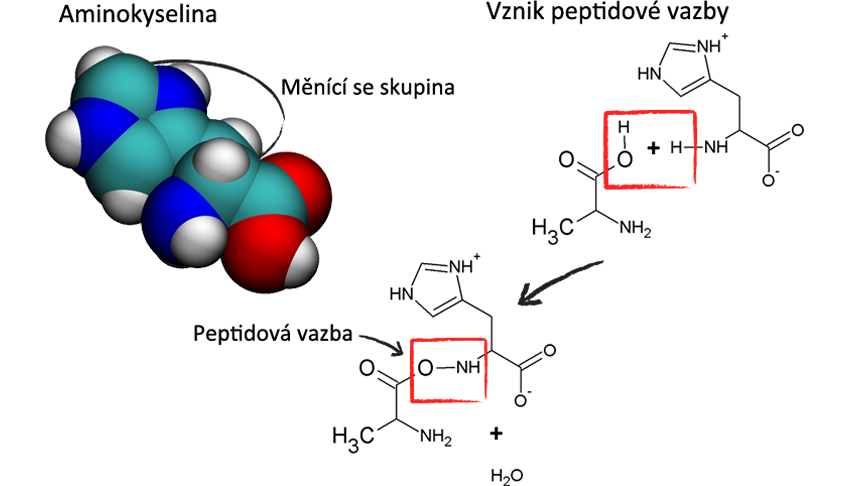
Jsou to velice tvárné molekuly, které mohou nabývat nespočet tvarů a funkcí, mohou být spojeny s jinými molekulami, např. s cukry - glykoproteiny nebo atomy kovů - hemoglobin. Bílkoviny jsou tvořeny řetězcem několika desítek až tisíců aminokyselin spojených za sebou. Těchto aminokyselin buňka využívá 20, což je pětkrát více, než využívá buňka bází pro stavbu nukleových kyselin.
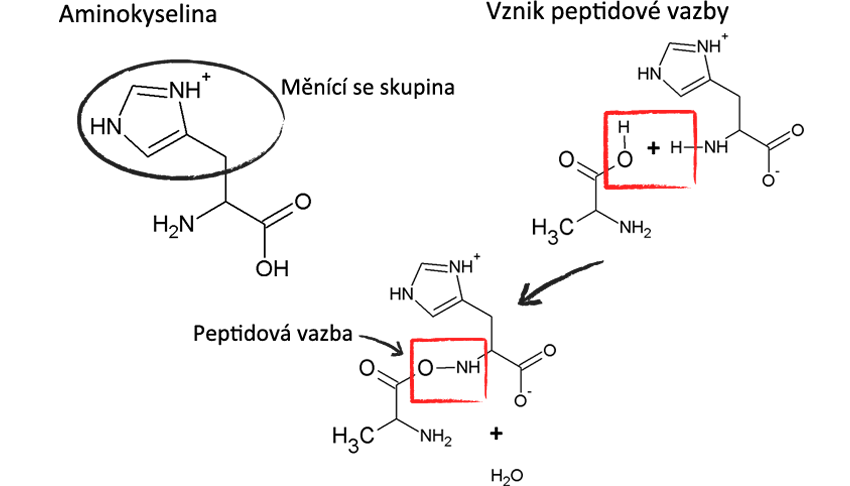
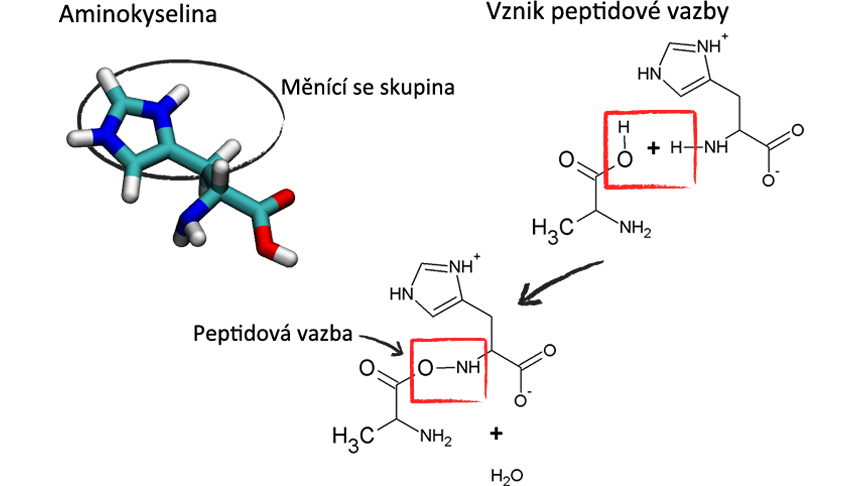
Pro vlastnosti bílkovin je důležitá právě tzv. primární struktura, tedy pořadí aminokyselin v molekule. Každá aminokyselina má dvě funkční skupiny: aminovou -NH2 a karboxylovou -COOH. K uhlíku, který je mezi těmito dvěma kyselinami, se připojují různé boční skupiny, jichž je v bílkovinách právě 20.
Tyto boční skupiny mají různé chemické složení i fyzikální vlastnosti: některé jsou hydrofilní, jiné hydrofobní, některé jsou za běžných podmínek nabité záporně, jiné kladně. Aminokyseliny se spojují do řetězců pomocí peptidové vazby, jejíž vznik je znázorněn na obrázku vpravo. Při vzniku této vazby se podobně jako při esterifikaci uvolní voda.
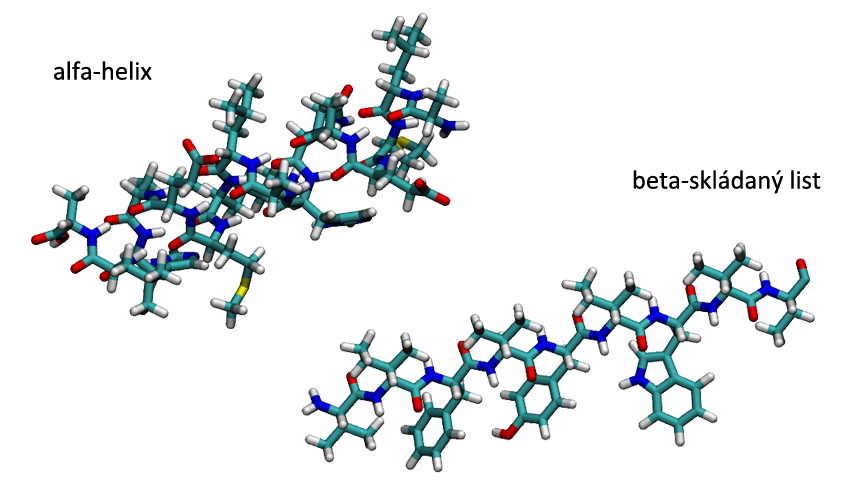
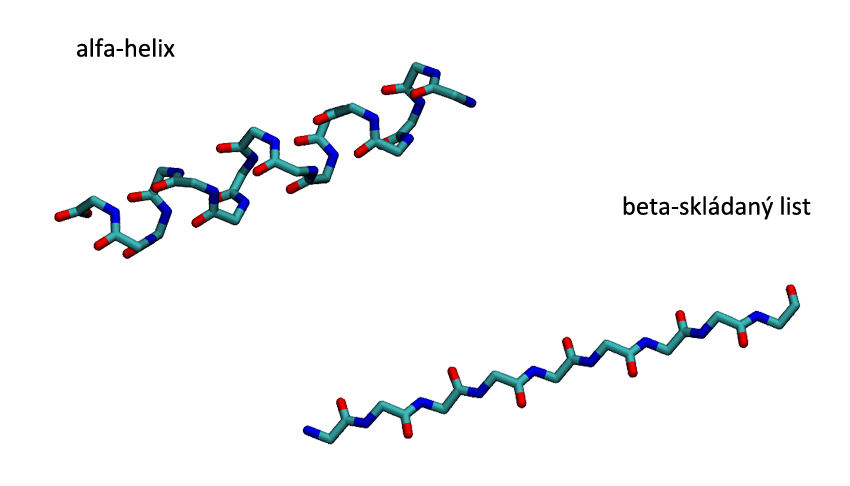
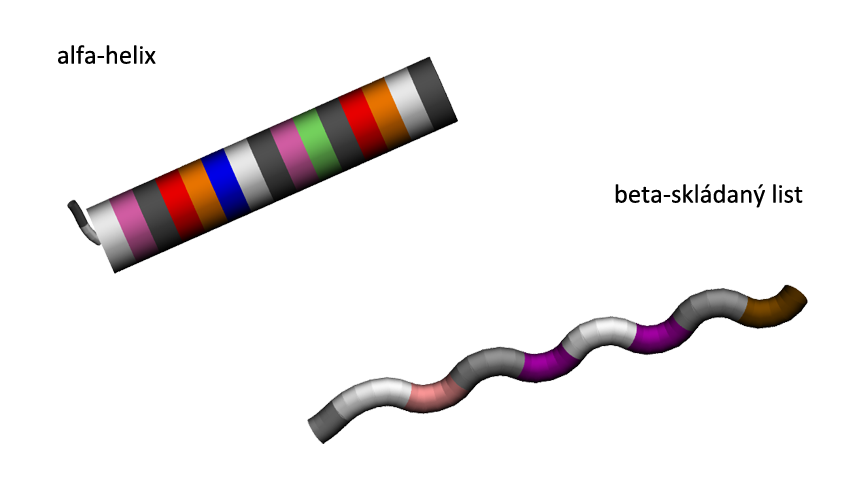
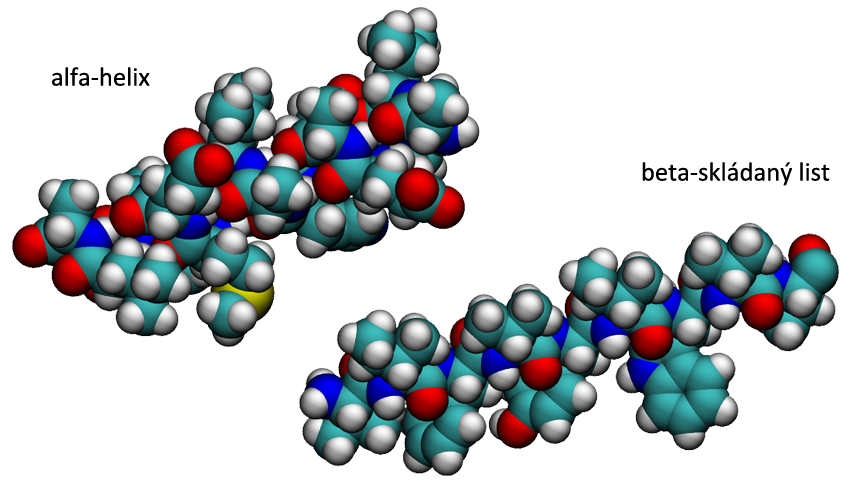
Díky velmi pružné kostře se mohou bílkoviny skládat do různých tvarů. Může jich být mnoho, ale jsou dva tvary, které se vyskytují v bílkovinách nejčastěji, tzv. alfa-helix a (beta-)skládaný list. V případě alfa-helixu jsou jednotlivá patra propojena vodíkovými vazbami a všechny boční řetězce směřují ven. Pro lepší zobrazení (a zjednodušení) se úseky s alfa-helixem zobrazují jako válec.
Druhá struktura skládaného listu je také stabilizována vodíkovými vazbami, ale na rozdíl od alfa-helixu jsou k ní potřeba dva řetězce, které probíhají vedle sebe a vytvářejí tuto strukturu. Ve zjednodušených modelech bývá zobrazována šipkou.
Přetažením báze napravo k bázi nalevo utvoř správné komplementární dvojice:
Přetáhni biomolekulu z pravé části do levé na místo, kde bys ji nejvíce očekával:
Správně!
Správně!